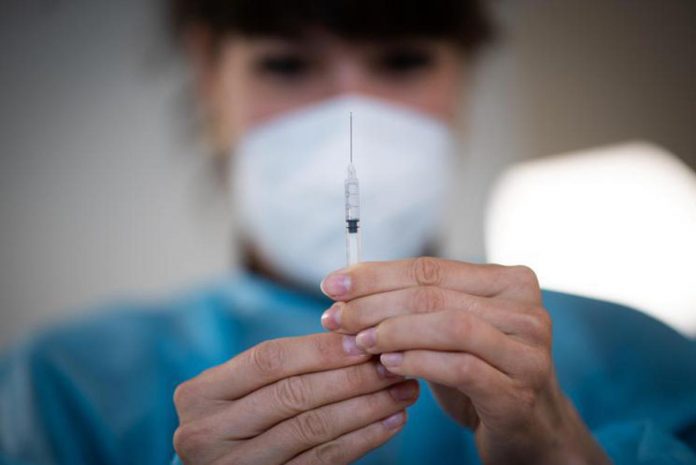
L’Aifa dice sì alla terza dose di vaccino. Si partirà dai “più fragili, quelli che dopo due dosi non hanno una risposta sufficiente” ha sottolineato il ministro della Salute Roberto Speranza annunciando che “nelle prossime ore ci sarà una circolare del capo Dipartimento della Prevenzione del ministero della Salute, Gianni Rezza, che indicherà esattamente quali sono queste categorie”.
La Commissione Tecnico Scientifica (Cts) dell’Aifa ha “espresso il proprio parere sulla somministrazione di dosi aggiuntive di vaccino contro il Covid-19” e ha ritenuto “appropriato, in attesa dell’autorizzazione di Ema, rendere disponibili i vaccini Comirnaty (Pfizer) e Spikevax (Moderna). Lo sottolinea una nota dell’Agenzia italiana del farmaco. La Cts, “rispondendo ai quesiti posti dal ministero della Salute” ha osservato “che la priorità della campagna vaccinale rimane il raggiungimento di un’elevata copertura vaccinale con il completamento dei cicli attualmente autorizzati per ridurre la circolazione del virus e lo sviluppo di varianti e prevenire efficacemente l’insorgenza di patologia grave e di decessi”.
La Cts ha stabilito che la ‘dose addizionale’ di vaccino Covid sarà somministrata “almeno 28 giorni dall’ultima somministrazione, a completamento del ciclo vaccinale nei soggetti adulti e adolescenti di età superiore ai 12 anni (vaccino Comirnaty) o sopra i 18 anni (vaccino Spikevax) in condizione di immunosoppressione clinicamente rilevante. Rientrano nella suddetta categoria i trapiantati di organo solido e i soggetti che presentino, sulla base della valutazione clinica, un livello di immunocompromissione assimilabile”.
Mentre come dose ‘booster’ “al fine di mantenere una efficace risposta immune al vaccino dopo il completamento del ciclo vaccinale” sarà somministrata “dopo almeno 6 mesi dall’ultima somministrazione, nei grandi anziani (over 80 anni) e nei soggetti ricoverati nelle Rsa – prosegue la nota – Tale opzione può essere resa disponibile anche agli operatori sanitari, a seconda del livello di esposizione all’infezione, del rischio individuale di sviluppare forme gravi di Covid-19 e in accordo alla strategia generale della campagna vaccinale”.
“Come dose aggiuntiva dovrebbe essere somministrato uno dei due vaccini a m-Rna autorizzati in Italia (Comirnaty* e Spikevax*). Qualora fosse stata eseguita una prima vaccinazione con vaccino adenovirale o nel caso in cui non fosse disponibile il medesimo vaccino a m-Rna utilizzato per le prime due dosi, si potrà ricorrere alla somministrazione di una dose aggiuntiva ‘eterologa’ con il tipo diverso di vaccino a m-Rna. In base alle conoscenze attuali il dosaggio raccomandato per la dose booster è uguale al dosaggio autorizzato per il ciclo primario”, si fa sapere inoltre. “La dose aggiuntiva – si evidenzia – dovrebbe essere somministrata dopo almeno sei mesi dall’ultima dose”.
“Aifa proprio oggi ha chiuso il suo lavoro della Cts” e “ha dato il via libera alla terza dose. Partiremo dai più fragili, quelli che dopo due dosi non hanno una risposta sufficiente”. “Nelle prossime ore ci sarà una circolare del capo Dipartimento della Prevenzione del ministero della Salute, Gianni Rezza, che indicherà esattamente quali sono queste categorie”, ha annunciato il ministro della Salute, Roberto Speranza, intervistato dal direttore de La Stampa Massimo Giannini, al Festival ‘Ritorno al futuro. La lezione di Covid e il domani che ci aspetta’, evento promosso da ‘Salute’, l’hub tematico del Gruppo Gedi, in corso a Villa Medici a Roma.
Anche l’Agenzia europea dei medicinali (Ema) ha dato il “via libera” lasciando però la scelta finale ai singoli governi. Gli stati dell’Ue possono partire con la terza dose del vaccino covid anche prima che si esprima l’Ema, l’agenzia europea del farmaco. “Gli Stati membri dell’Unione europea, attraverso i loro gruppi consultivi tecnici nazionali sull’immunizzazione (Nitag), possono procedere comunque nel pianificare campagne di somministrazione di dosi aggiuntive o dosi ‘booster'” di vaccino anti-Covid, “come misura proattiva di salute pubblica, anche prima che una decisione regolatoria venga presa. Questo tipo di scelte sono pienamente comprese dall’agenzia nel contesto di emergenza in cui siamo”, ha spiegato Marco Cavaleri, responsabile Vaccini e Prodotti terapeutici per Covid-19 dell’Agenzia europea del farmaco Ema, durante un briefing per la stampa.